ATOMLARDA ENERJİ SEVİYELERİ VE BANT YAPILARI
Bir maddeyi elektriksel bakımdan iletken hâle getirebilmek için dışarıdan bir enerji uygulanması gerekir. Bu enerji miktarı üç ayrı enerji bandının oluşmasını sağlar. Resim-1'de gösterilmiştir. Herhangi bir atomun valans bandındaki elektronların yörüngesinden koparak iletkenlik bandına geçebilmesi için, bu iki bant arasındaki yasak bandı geçmesi gerekir.
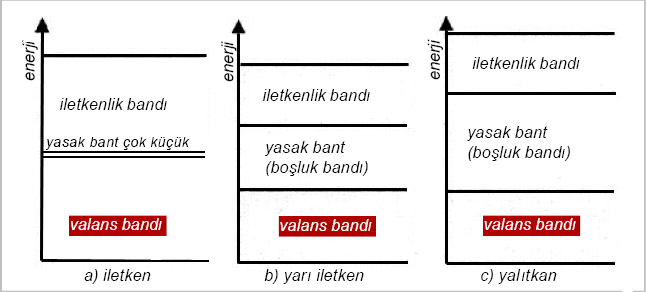
a. Yasak bant: Elektron bakımından boş bulunan ve valans bandındaki elektronların iletkenlik bandına geçmesini zorlaştıran boşluğa denir.
b. İletkenlik bandı: Valans bandından kopan ve akım taşıyabilecek durumda olan elektronların bulunduğu banttır. Maddeler, elektronlarının bu banda geçmesiyle iletken hâle gelirler.
c. Atomların yörüngelerindeki elektron sayıları: 20. yüzyılın başlarında Bohr ve diğer bilginler tarafından yapılan çalışmalar elektron yörüngelerinin katmanlar hâlinde oluştuğunu göstermiştir. Başka bir deyişle, elektronlar yörünge (orbital, kabuk) adı verilen yollar üzerinde dönerler. Bu yörüngelere K, L, M, N, O, P, Q adı verilir ve yörüngeler çekirdekten dışarıya doğru 1, 2, 3, ... olarak numaralanır. Her yörüngede en çok kaç elektron bulunduğu katman sayısının karesinin 2 ile çarpılmasıyla bulunur. Yani her katmanda bulunabilen en fazla elektron sayısı 2n2 denklemiyle bulunur (n = 1, 2, 3 ...). Atomların kabuklarındaki maksimum elektron sayıları şöyledir:
K: 2, L: 8, M: 18, N: 32, O: 50, P: 72, Q: 98
Animasyon-1'de Kalsiyum atomuna kadar olan atomların peryodik tablodaki yerleri gösterilmiştir. İlk dört yörüngedeki elektron sayılarını görebilirsiniz.
ç. Atomlarda kovalent (ikili) bağ: Kristal özellikli maddelerin içinde bulunan atomların elektronları dizilirken kimyasal olarak 8'li bağlarla birbirine bağlanırlar. Yani kovalent yapının oluşması için 8 elektrona gerek vardır. Ve bu işlem yarı iletken atomlarının son yörüngelerindeki elektronların karşılıklı kullanımıyla gerçekleşir. Animasyon-2'de germanyum atomunda kovalent bağın oluşumu gösterilmiştir. Ortak kullanımdaki elektronlar hem kendi hem de komşu atomun çevresinde döner. Buna kovalent bağ denir. Silisyum ya da germanyum kristali ısıtılır ya da elektrik akımının etkisine maruz bırakılırsa, kovalent bağların çekim kuvvetini yenen çok az sayıdaki elektron serbest hâle geçer.